Critères d’inclusion :
- Âge ≥ 18 ans
- Allo-GCSH avec tout type de donneur, source de cellules souches, prophylaxie de la GvH ou schéma de conditionnement
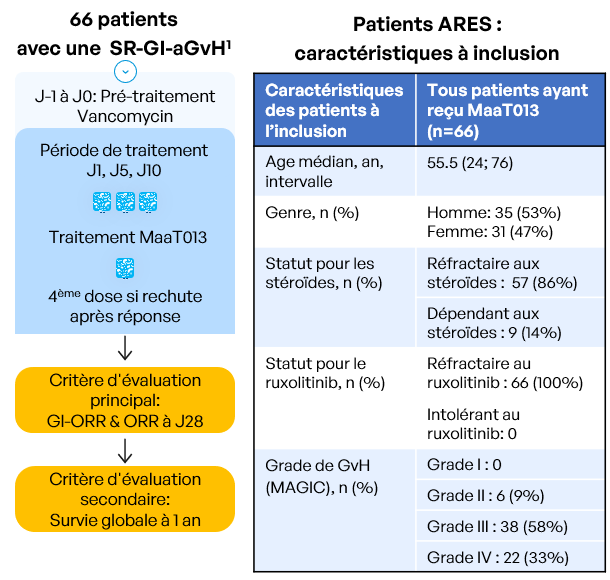
- Patients développant un épisode d’aGvH avec atteinte gastro-intestinale selon les directives MAGIC (grades II à IV), avec ou sans atteinte d’autres organes (Harris et al., 2016)
- Patients résistants aux corticoïdes ET soit résistants à OU intolérants au ruxolitinib (patients intolérants : ayant présenté un événement indésirable de grade 3 ou plus, apparu sous traitement et attribué au ruxolitinib, qui n’a pas été résolu dans les 7 jours suivant l’arrêt du ruxolitinib). Le diagnostic doit être confirmé dans les 48 heures précédant le début du pré-traitement de l’étude.